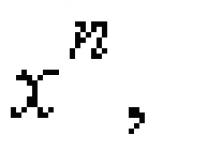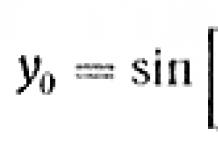Основание однородное - – естественное основание, сложенное горной породой одного вида. [Терминологический словарь по строительству на 12 языках (ВНИИИС Госстроя СССР)] Рубрика термина: Горные породы Рубрики энциклопедии: Абразивное оборудование, Абразивы,… …
Основание - – поверхность, на которую наклеивают стеновое покрытие, например стена или потолок. [ГОСТ Р 52805 2007] Рубрика термина: Обои Рубрики энциклопедии: Абразивное оборудование, Абразивы, Автодороги, Автотехника … Энциклопедия терминов, определений и пояснений строительных материалов
Наука о методах определения химического состава веществ. Химический анализ буквально пронизывает всю нашу жизнь. Его методами проводят скрупулезную проверку лекарственных препаратов. В сельском хозяйстве с его помощью определяют кислотность почв… … Энциклопедия Кольера
Харько, Харьков (Харитон) мифический персонаж казак Харько, Харьков Имя при рождении: вероятно, Харитон … Википедия
Неорганическая химия раздел химии, связанный с изучением строения, реакционной способности и свойств всех химических элементов и их неорганических соединений. Это область охватывает все химические соединения, за исключением органических… … Википедия
Изучение химии в России формально ведет свое начало с учреждения в 1725 г. в СПб. Академии наук. В 1727 г. в качестве натуралиста и химика был приглашен сын тюбингенского аптекаря Иоганн Георг Гмелин, проведший почти все время своего пребывания в … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
В Викисловаре есть статья «органическая химия» Органическая химия раздел химии, изучающий со … Википедия
Однокислотные (NaOH , КОН, NH 4 OH и др.);
Двухкислотные (Са(ОН) 2 , Cu(OH) 2 , Fe(OH) 2 ;
Трехкислотные (Ni(OH) 3 , Со(ОН) 3 , Мn(ОН) 3 .
Классификация по растворимости в воде и степени ионизации:
Растворимые в воде сильные основания,
например:
щелочи - гидроксиды щелочных и щелочноземельных металлов LiOH - гидроксид лития, NaOH - гидроксид натрия (едкий натр), КОН - гадроксид калия (едкое кали), Ва(ОН) 2 - гидроксид бария;
Нерастворимые в воде сильные основания,
например:
Сu(ОН) 2 - гидроксид меди (II), Fe(OH) 2 - гидроксид железа (II), Ni(OH) 3 - гидроксид никеля (III).
Химические свойства
1. Действие на индикаторы
Лакмус - синий;
Метилоранж - жёлтый,
Фенолфталеин - малиновый.
2. Взаимодействие с кислотными оксидами
2KOH + CO 2 = K 2 CO 3 + H 2 O
KOH + CO 2 = KHCO 3
3. Взаимодействие с кислотами (реакция нейтрализации)
NaOH + HNO 3 = NaNO 3 + H 2 O; Cu(OH) 2 + 2HCl = CuCl 2 + 2H 2 O
4. Обменная реакция с солями
Ba(OH) 2 + K 2 SO 4 = 2KOH + BaSO 4
3KOH + Fe(NO 3) 3 = Fe(OH) 3 + 3KNO 3
5. Термический распад
Cu(OH) 2 t = CuO + H 2 O; 2 CuOH = Cu 2 O + Н 2 O
2Со(ОН) 3 = Со 2 O 3 + ЗН 2 O; 2АgОН = Аg 2 O + Н 2 O
6. Гидроксиды, в которых d-металлы имеют низкие с. о., способны окисляться кислородом воздуха,
например:
4Fe(OH) 2 + O 2 + 2Н 2 O = 4Fe(OH) 3
2Мn(OН) 2 + O 2 + 2Н 2 O = 2Мn(ОН) 4
7. Растворы щелочей взаимодействуют c амфотерными гидроксидами:
2КОН + Zn(OH) 2 = К 2
2КОН + Al 2 O 3 + ЗН 2 O = 2К
8. Растворы щелочей взаимодействуют с металлами, образующими амфотерные оксиды игидроксиды (Zn , AI и др.),
например:
Zn + 2 NaOH +2Н 2 O = Na 2 + Н 2
2AI +2КOН + 6Н 2 O= 2КAl(ОН) 4 ] + 3H 2
9. В растворах щелочей некоторые неметаллы диспропорционируют,
например:
Cl 2 + 2NaOH = NaCl + NaCIO + Н 2 O
3S+ 6NaOH = 2Na 2 S+ Na 2 SO 3 + 3H 2 O
4P+ 3KOH + 3H 2 O = PH 3 + 3KH 2 PO 2
10. Растворимые основания широко используются в реакциях щелочного гидролиза различных органических соединений (галогенопроизводных углеводородов, сложных эфиров, жиров и др.),
например:
C 2 H 5 CI + NaOH = С 2 Н 5 ОН + NaCl
Способы получения щелочей и нерастворимых оснований
1. Реакции активных металлов (щелочных и щелочноземельных металлов) с водой:
2Na + 2H 2 O = 2 NaOH + H 2
Ca + 2H 2 O = Ca(OH) 2 + H 2
2. Взаимодействие оксидов активных металлов с водой:
BaO + H 2 O = Ba(OH) 2
3. Электролиз водных растворов солей:
2NaCl + 2H 2 O = 2NaOH + H 2 + Cl 2
CaCI 2 + 2Н 2 O = Са(ОН) 2 +Н 2 + Cl 2
4. Осаждение из растворов соответствующих солей щелочами:
CuSO 4 + 2NaOH = Cu(OH) 2 + Na 2 SO 4
FeCI 3 + 3KOH = Fe(OH) 3 + 3KCI
ОПРЕДЕЛЕНИЕ
Основаниями называются электролиты, при диссоциации которых из отрицательных ионов образуются только ионы OH — :
Fe(OH) 2 ↔ Fe 2+ + 2OH — ;
NH 3 + H 2 O ↔ NH 4 OH ↔ NH 4 + + OH — .
Все неорганические основания классифицируют на растворимые в воде (щелочи) – NaOH, KOH и нерастворимые в воде (Ba(OH) 2 , Ca(OH) 2). В зависимости от проявляемых химических свойств среди оснований выделяют амфотерные гидроксиды.
Химические свойства оснований
При действии индикаторов на растворы неорганических оснований происходит изменение их окраски, так, при попадании в раствор основания лакмус приобретает синюю окраску, метилоранж – жёлтую, а фенолфталеин – малиновую.
Неорганические основания способны реагировать с кислотами с образованием соли и воды, причем, нерастворимые в воде основания взаимодействуют только с растворимыми в воде кислотами:
Cu(OH) 2 ↓ + H 2 SO 4 = CuSO 4 +2H 2 O;
NaOH + HCl = NaCl + H 2 O.
Нерастворимые в воде основания термически неустойчивы, т.е. при нагревании они подвергаются разложению с образованием оксидов:
2Fe(OH) 3 = Fe 2 O 3 + 3 H 2 O;
Mg(OH) 2 = MgO + H 2 O.
Щелочи (растворимые в воде основания) взаимодействуют с кислотными оксидами с образованием солей:
NaOH + CO 2 = NaHCO 3 .
Щелочей также способны вступать в реакции взаимодействия (ОВР) с некоторыми неметаллами:
2NaOH + Si + H 2 O → Na 2 SiO 3 +H 2 .
Некоторые основания вступают в реакции обмена с солями:
Ba(OH) 2 + Na 2 SO 4 = 2NaOH + BaSO 4 ↓.
Амфотерные гидроксиды (основания) проявляют также свойства слабых кислот и реагируют с щелочами:
Al(OH) 3 + NaOH = Na.
К амфотерным основаниям относятся гидроксиды алюминия, цинка. хрома (III) и др.
Физические свойства оснований
Большинство оснований – твердые вещества, которые характеризуются различной растворимостью в воде. Щелочи – растворимые в воде основания – чаще всего твердые вещества белого цвета. Нерастворимые в воде основания могут иметь различную окраску, например, гидроксид железа (III)- твердое вещество бурого цвета, гидроксид алюминия – твердое вещество белого цвета, а гидроксид меди (II) – твердое вещество голубого цвета.
Получение оснований
Основания получают разными способами, например, по реакции:
— обмена
CuSO 4 + 2KOH → Cu(OH) 2 ↓ + K 2 SO 4 ;
K 2 CO 3 + Ba(OH) 2 → 2KOH + BaCO 3 ↓;
— взаимодействия активных металлов или их оксидов с водой
2Li + 2H 2 O→ 2LiOH +H 2 ;
BaO + H 2 O→ Ba(OH) 2 ↓;
— электролиза водных растворов солей
2NaCl + 2H 2 O = 2NaOH + H 2 + Cl 2 .
Примеры решения задач
ПРИМЕР 1
| Задание | Вычислите практическую массу оксида алюминия (выход целевого продукта составляет 92%) по реакции разложения гидроксида алюминия массой 23,4 г. |
| Решение |
Запишем уравнение реакции:
2Al(OH) 3 = Al 2 O 3 + 3H 2 O. Молярная масса гидроксида алюминия, рассчитанная с использованием таблицы химических элементов Д.И. Менделеева – 78 г/моль. Найдем количество вещества гидроксида алюминия: v(Al(OH) 3) = m(Al(OH) 3)/M(Al(OH) 3); v(Al(OH) 3) = 23,4/78 = 0,3 моль. Согласно уравнению реакции v(Al(OH) 3): v(Al 2 O 3) = 2:1, следовательно, количество вещества оксида алюминия составит: v(Al 2 O 3) = 0,5 × v(Al(OH) 3); v(Al 2 O 3) = 0,5 ×0,3 = 0,15 моль. Молярная масса оксида алюминия, рассчитанная с использованием таблицы химических элементов Д.И. Менделеева – 102 г/моль. Найдем теоретическую массу оксида алюминия: m(Al 2 O 3) th = 0,15×102 = 15,3 г. Тогда, практическая масса оксида алюминия составляет: m(Al 2 O 3) pr = m(Al 2 O 3) th × 92/100; m(Al 2 O 3) pr = 15,3×0,92 = 14 г. |
| Ответ | Масса оксида алюминия — 14 г. |
ПРИМЕР 2
| Задание |
Осуществите ряд превращений:
Fe→ FeCl 2 → Fe(OH) 2 →Fe(OH) 3 →Fe(NO 3) 3 |
Один из классов сложных неорганических веществ - основания. Это соединения, включающие атомы металла и гидроксильную группу, которая может отщепляться при взаимодействии с другими веществами.
Строение
Основания могут содержать одну или несколько гидроксо-групп. Общая формула оснований - Ме(ОН) х. Атом металла всегда один, а количество гидроксильных групп зависит от валентности металла. При этом валентность группы ОН всегда I. Например, в соединении NaOH валентность натрия равна I, следовательно, присутствует одна гидроксильная группа. В основании Mg(OH) 2 валентность магния - II, Al(OH) 3 валентность алюминия - III.
Количество гидроксильных групп может меняться в соединениях с металлами с переменной валентностью. Например, Fe(OH) 2 и Fe(OH) 3 . В таких случаях валентность указывается в скобках после названия - гидроксид железа (II), гидроксид железа (III).
Физические свойства
Характеристика и активность основания зависит от металла. Большинство оснований - твёрдые вещества белого цвета без запаха. Однако некоторые металлы придают веществу характерную окраску. Например, CuOH имеет жёлтый цвет, Ni(OH) 2 - светло-зелёный, Fe(OH) 3 - красно-коричневый.

Рис. 1. Щёлочи в твёрдом состоянии.
Виды
Основания классифицируются по двум признакам:
- по количеству групп ОН - однокислотные и многокислотные;
- по растворимости в воде - щёлочи (растворимые) и нерастворимые.
Щёлочи образуются щелочными металлами - литием (Li), натрием (Na), калием (K), рубидием (Rb) и цезием (Cs). Кроме того, к активным металлам, образующим щёлочи, относят щелочноземельные металлы - кальций (Ca), стронций (Sr) и барий (Ba).
Эти элементы образуют следующие основания:
- LiOH;
- NaOH;
- RbOH;
- CsOH;
- Ca(OH) 2 ;
- Sr(OH) 2 ;
- Ba(OH) 2 .
Все остальные основания, например, Mg(OH) 2 , Cu(OH) 2 , Al(OH) 3 , относятся к нерастворимым.
По-другому щёлочи называются сильными основаниями, а нерастворимые - слабыми основаниями. При электролитической диссоциации щёлочи быстро отдают гидроксильную группу и быстрее вступают в реакцию с другими веществами. Нерастворимые или слабые основания менее активные, т.к. не отдают гидроксильную группу.

Рис. 2. Классификация оснований.
Особое место в систематизации неорганических веществ занимают амфотерные гидроксиды. Они взаимодействуют и с кислотами, и с основаниями, т.е. в зависимости от условий ведут себя как щёлочь или как кислота. К ним относятся Zn(OH) 2 , Al(OH) 3 , Pb(OH) 2 , Cr(OH) 3 , Be(OH) 2 и другие основания.
Получение
Основания получают различными способами. Самый простой - взаимодействие металла с водой:
Ba + 2H 2 O → Ba(OH) 2 + H 2 .
Щёлочи получают в результате взаимодействия оксида с водой:
Na 2 O + H 2 O → 2NaOH.
Нерастворимые основания получаются в результате взаимодействия щелочей с солями:
CuSO 4 + 2NaOH → Cu(OH) 2 ↓+ Na 2 SO 4 .
Химические свойства
Основные химические свойства оснований описаны в таблице.
|
Реакции |
Что образуется |
Примеры |
|
С кислотами |
Соль и вода. Нерастворимые основания взаимодействуют только с растворимыми кислотами |
Cu(OH) 2 ↓ + H 2 SO 4 → CuSO 4 +2H 2 O |
|
Разложение при высокой температуре |
Оксид металла и вода |
2Fe(OH) 3 → Fe 2 O 3 + 3H 2 O |
|
С кислотными оксидами (реагируют щёлочи) |
NaOH + CO 2 → NaHCO 3 |
|
|
С неметаллами (вступают щёлочи) |
Соль и водород |
2NaOH + Si + H 2 O → Na 2 SiO 3 +H 2 |
|
Обмена с солями |
Гидроксид и соль |
Ba(OH) 2 + Na 2 SO 4 → 2NaOH + BaSO 4 ↓ |
|
Щелочей с некоторыми металлами |
Сложная соль и водород |
2Al + 2NaOH + 6H 2 O → 2Na + 3H 2 |
С помощью индикатора проводится тест на определение класса основания. При взаимодействии с основанием лакмус становится синим, фенолфталеин - малиновым, метилоранж - жёлтым.

Рис. 3. Реакция индикаторов на основания.
Что мы узнали?
Из урока 8 класса химии узнали об особенностях, классификации и взаимодействии оснований с другими веществами. Основания - сложные вещества, состоящие из металла и гидроксильной группы ОН. Они делятся на растворимые или щёлочи и нерастворимые. Щёлочи - более агрессивные основания, быстро реагирующие с другими веществами. Основания получают при взаимодействии металла или оксида металла с водой, а также в результате реакции соли и щёлочи. Основания реагируют с кислотами, оксидами, солями, металлами и неметаллами, а также разлагаются при высокой температуре.
Тест по теме
Оценка доклада
Средняя оценка: 4.5 . Всего получено оценок: 259.
Основания – сложные вещества, состоящие из атома металла и одной или нескольких гидроксильных групп. Общая формула оснований Ме(ОН) n . Основания (с точки зрения теории электролитической диссоциации) – это электролиты, диссоциирующие при растворении в воде с образованием катионов металла и гидроксид-ионов ОН – .
Классификация. По растворимости в воде основания делят на щелочи (растворимые в воде основания) и нерастворимые в воде основания . Щелочи образуют щелочные и щелочно-земельные металлы, а также некоторые другие элементы-металлы. По кислотности (числу ионов О Н – , образующихся при полной диссоциации, или количеству ступеней диссоциации) основания подразделяют на однокислотные (при полной диссоциации получается один ион О Н – ; одна ступень диссоциации) и многокислотные (при полной диссоциации получается больше одного иона О Н – ; более одной ступени диссоциации). Среди многокислотных оснований различают двухкислотные (например, Sn(OH) 2 ), трехкислотные (Fe(OH) 3) и четырехкислотные (Th(OH) 4). Однокислотным является, например, основание КОН.
Выделяют группу гидроксидов, которые проявляют химическую двойственность. Они взаимодействую как с основаниями, так и с кислотами. Это амфотерные гидроксиды (см. таблицу 1) .
Таблица 1 - Амфотерные гидроксиды
|
Амфотерный гидроксид (основная и кислотная форма) |
Кислотный остаток и его валентность |
Комплексный ион |
|
Zn(OH) 2 / H 2 ZnO 2 |
ZnO 2 (II) |
2– |
|
Al(OH) 3 / HAlO 2 |
AlO 2 (I) |
– , 3– |
|
Be(OH) 2 / H 2 BeO 2 |
BeO 2 (II) |
2– |
|
Sn(OH) 2 / H 2 SnO 2 |
SnO 2 (II) |
2– |
|
Pb(OH) 2 / H 2 PbO 2 |
PbO 2 (II) |
2– |
|
Fe(OH) 3 / HFeO 2 |
FeO 2 (I) |
– , 3– |
|
Cr(OH) 3 / HCrO 2 |
CrO 2 (I) |
– , 3– |
Физические свойства. Основания - твердые вещества различных цветов и различной растворимости в воде.
Химические свойства оснований
1) Диссоциация : КОН + n Н 2 О К + × m Н 2 О + ОН – × d Н 2 О или сокращенно: КОН К + + ОН – .
Многокислотные основания диссоциируют по нескольким ступеням (в основном диссоциация протекает по первой ступени). Например, двухкислотное основание Fe(OH) 2 диссоциирует по двум ступеням:
Fe(OH) 2 FeOH + + OH – (1 ступень);
FeOH + Fe 2+ + OH – (2 ступень).
2) Взаимодействие с индикаторами (щелочи окрашивают фиолетовый лакмус в синий цвет, метилоранж – в желтый, а фенолфталеин – в малиновый):
индикатор + ОН – (щелочь )окрашенное соединение.
3 ) Разложение с образованием оксида и воды (см. таблицу 2 ). Гидроксиды щелочных металлов устойчивы к нагреванию (плавятся без разложения). Гидроксиды щелочно-земельных и тяжелых металлов обычно легко разлагаются. Исключение составляет Ba(OH) 2 , у которого t разл достаточно высока (примерно 1000 ° C ).
Zn(OH) 2 ZnO + H 2 O .
Таблица 2 - Температуры разложения некоторых гидроксидов металлов
| Гидроксид | t разл , ° C | Гидроксид | t разл , ° C | Гидроксид | t разл , ° C |
| LiOH | 925 | Cd(OH) 2 | 130 | Au(OH) 3 | 150 |
| Be(OH) 2 | 130 | Pb(OH) 2 | 145 | Al (OH) 3 | >300 |
| Ca(OH) 2 | 580 | Fe(OH) 2 | 150 | Fe(OH) 3 | 500 |
| Sr(OH) 2 | 535 | Zn (OH) 2 | 125 | Bi (OH) 3 | 100 |
| Ba(OH) 2 | 1000 | Ni (OH) 2 | 230 | In (OH) 3 | 150 |
4 ) Взаимодействие щелочей с некоторыми металлами (например, Al и Zn ):
В растворе: 2Al + 2NaOH + 6H 2 O ® 2Na + 3H 2
2Al + 2OH – + 6H 2 О ® 2 – + 3H 2 .
При сплавлении: 2Al + 2NaOH + 2H 2 O 2NaAl О 2 + 3H 2 .
5 ) Взаимодействие щелочей с неметаллами :
6 NaOH + 3Cl 2 5Na Cl + NaClO 3 + 3H 2 O .
6) Взаимодействие щелочей с кислотными и амфотерными оксидами :
2NaOH + СО 2 ® Na 2 CO 3 + H 2 O 2OH – + CO 2 ® CO 3 2– + H 2 O .
В растворе: 2NaOH + ZnO + H 2 O ® Na 2 2OH – + ZnO + H 2 О ® 2– .
При сплавлении с амфотерным оксидом: 2NaOH + ZnO Na 2 ZnO 2 + H 2 O .
7) Взаимодействие оснований с кислотами :
H 2 SO 4 + Ca(OH) 2 ® CaSO 4 ¯ + 2H 2 O 2H + + SO 4 2– + Ca 2+ +2OH – ® CaSO 4 ¯ + 2H 2 O
H 2 SO 4 + Zn(OH) 2 ® ZnSO 4 + 2H 2 O 2H + + Zn(OH) 2 ® Zn 2+ + 2H 2 O.
8) Взаимодействие щелочей с амфотерными гидроксидами (см. таблицу 1 ):
В растворе: 2NaOH + Zn(OH) 2 ® Na 2 2OH – + Zn(OH) 2 ® 2–
При сплавлении: 2NaOH + Zn(OH) 2 Na 2 ZnO 2 + 2H 2 O .
9 ) Взаимодействие щелочей с солями. В реакцию вступают соли, которым соответствует нерастворимое в воде основание :
CuS О 4 + 2NaOH ® Na 2 SO 4 + Cu(OH) 2 ¯ Cu 2+ + 2OH – ® Cu(OH) 2 ¯ .
Получение. Нерастворимые в воде основания получают путем взаимодействия соответствующей соли со щелочью:
2NaOH + ZnS О 4 ® Na 2 SO 4 + Zn(OH) 2 ¯ Zn 2+ + 2OH – ® Zn(OH) 2 ¯ .
Щелочи получают :
1) Взаимодействием оксида металла с водой :
Na 2 O + H 2 O ® 2NaOH CaO + H 2 O ® Ca(OH) 2 .
2) Взаимодействием щелочных и щелочно-земельных металлов с водой :
2Na + H 2 O ® 2NaOH + H 2 Ca + 2H 2 O ® Ca(OH) 2 + H 2 .
3) Электролизом растворов солей :
2NaCl + 2H 2 O H 2 + 2NaOH + Cl 2 .
4 ) Обменным взаимодействием гидроксидов щелочно-земельных металлов с некоторыми солями . В ходе реакции должна обязательно получаться нерастворимая соль .
Ba(OH) 2 + Na 2 CO 3 ® 2NaOH + BaCO 3 ¯ Ba 2 + + CO 3 2 – ® BaCO 3 ¯ .
Л.А. Яковишин